锌电极添加剂及电解液添加剂研究进展
2016-12-28
中国电源产业网

导语:碱性锌电极具有广泛的市场应用,但因其在充放电过程中容易产生锌枝晶且易钝化或被腐蚀、变形严重等限制了其发展,无汞添加剂的研究便成了科研一大热点。本文从锌电极变形、锌枝晶产生、电极钝化、腐蚀四种机理及电极添加剂、电解液添加剂、复配添加剂三个方面综述了锌电池添加剂的研究现状,为无汞锌电池的研发提供有价值的信息。
摘 要:碱性锌电极具有广泛的市场应用,但因其在充放电过程中容易产生锌枝晶且易钝化或被腐蚀、变形严重等限制了其发展,无汞添加剂的研究便成了科研一大热点。本文从锌电极变形、锌枝晶产生、电极钝化、腐蚀四种机理及电极添加剂、电解液添加剂、复配添加剂三个方面综述了锌电池添加剂的研究现状,为无汞锌电池的研发提供有价值的信息。
关键词:锌电极;代汞;添加剂
The Development of Zinc Electrode
on Electrode Additives and Electrolyte Additives
Fan zhao bao1 LIUlijuan2 Heyubin3
(3401 Factory China Aerospace Science and Industry Corporation Zunyi 563003)
Abstract:Alkaline zinc batteries are widely used in market. However, the problems of dendrite growth、passivation、self-corrosion and deformation during charge and discharge limit its development, as a result, additive without mercury become a hot research topic recently. In the paper, present researches situation of zinc electrode are discussed from four mechanism of zinc electrode deformation、dendrite growth、passivation、self-corrosion and three aspects of electrode additives、electrolyte additives as well as composite additives , which will provide valuable informations for the development of zinc batteries without mercury .
Keywords: zinc electrode; substitute for mercury; additives
1引言
金属锌作为碱性电池的负极活性物质,具有较高的比能量和比功率,电极电势较负,其阳极溶解反应极化较小,电化学当量较低,电极过程可逆,且锌资源丰富,成本低,无毒性。
尽管如此,由于锌本身的热力学不稳定性,化学活泼性,锌电极在充放电过程中容易产生锌枝晶且易钝化或被腐蚀、变形严重。通常,人们主要从以下几个方面研究来改善锌电极的性能:(1)改进电极结构,使溶解的锌保持在原结构上;(2)在电极中加入金属或金属氧化物添加剂;(3)在电解液中加入有机物添加剂或有机与无机添加剂联合使用使其吸附在锌电极表面,抑制或减缓锌枝晶的生长。
在工程实际应用中,主要采取的手段是在锌电极中加入单质汞或氧化汞使锌电极汞齐化来抑制锌电极的自放电。但由于汞具有毒性,无汞电池的研制成为迫在眉睫的问题。另外有研究[1]发现,在二次电池锌电极中加入汞后,促进了电极变形,使其循环寿命降低。近年来,锌电极代汞添加剂及电解液添加剂研究越来越多。
2机理分析
2.1锌电极变形机理
锌电极经过多次的充放电循环后由于放电过程形成的ZnO或Zn(OH)2溶解在电解液中从而形成锌酸盐,在循环过程中活性物质重新分布而不能回到原来的位置,造成锌电极变形。
对于变形产生的原因,通过长期以来人们的大量研究,提出了较为经典的Choi的隔膜传输模型[2]、Mcbreen的浓差极化电池模型[3]以及Einerhand的密度梯度模型[4]。Choi等认为电解质组分通过隔膜的渗透以及电渗透力而产生平行于电极表面的对流传质,并且在充、放电过程中锌酸盐的对流方向正好相反,充电时锌酸盐从中心传到边缘的量很少,放电时相反,从而造成锌电极变形,但是该模型不能解释无隔膜体系中的锌电极变形;Mcbreen认为在充放电过程中非均匀分布的电流密度以及不同的极化度,导致了在锌电极表面产生浓差电池,因此使得活性物质逐渐从电极的边缘向中心聚集,从而出现形变,但是有研究认为,浓差电池不是促使锌电极重新分布的唯一原因;Einerhand认为变形是由浓度梯度引起的,在充电过程中锌转移量小于在放电过程中锌转移的量,锌酸盐密度大,容易沉积在底部,该模型仅是定性的讨论,尚无令人信服的依据。
2.2锌枝晶生成机理
在充电过程中,锌容易沉积在电极表面突出的部分,从而形成枝晶。关于枝晶形成的机制人们进行了较为深入的研究[5-7]。充电过程中电极表面附近薄液层中反应离子较贫乏,浓差极化较大,反应物离子扩散到电极表面突出处要比其他位置更加容易,造成突出处的沉积速率较其他位置大,结果形成枝晶。
2.3锌电极钝化机理
关于锌阳极钝化的机理[8],往往由于实验条件的不同,得到的结论不一致。当锌电极阳极溶解时,电极表面附近溶液中锌酸盐浓度逐渐增大。当锌酸盐达到饱和时,电极表面开始生成ZnO或Zn(OH)2固态沉积物,减小了电极的有效表面积,极化加剧,电极电势迅速向正向移动。当电极电势增大到生成吸附ZnO的电极电势时,锌电极表面生成紧密的ZnO吸附层,大大提高了锌阳极溶解过程的活化能,致使锌的阳极溶解受到很大的阻滞而进入钝态。
2.3锌电极腐蚀机理
由于金属的自溶解和氢的析出在金属表面上同时发生,必然处在同一电极电势下。这一电势不是金属的平衡电势,也不是氢的平衡电势,而是介于它们之间,称为混合电势。这种关系可用极化曲线表示,如图1所示。
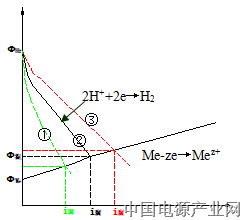
图1金属自溶解示意图
阴极极化曲线表示金属上析出氢,由于超电势较高,所以曲线较陡。阳极极化曲线表示金属自溶解,由于超电势较小,所以曲线较为平缓。两条极化曲线的交点在横轴对应的电流,称为金属自溶电流或氢析出电流,有时也称为腐蚀电流。此交点对应的纵轴电势称为混合电势。
如果在主体金属中含有氢超电势低的金属,将会加速主体金属的自溶速率。阴极极化曲线将会变得平缓一些,如图中③所示,从而使自溶电流增大。反之,含有超电势高的金属,自溶电流将会减小。
固体锌与碱溶液接触时,在热力学上是不稳定的。因为锌有较高的氢过电位,比氢气析出所需的电位约低0.4V,因此,锌会产生腐蚀(即自溶解)。锌在碱液中的腐蚀,实际上是锌的溶解和氢的析出这一对共轭反应的共同作用:
2H2O-2e→H2+2OH- E0=-0.83V
Zn+4OH-→Zn(OH)42-+2e E0=-1.22V
由于锌表面的不均匀性,各点的电化学活性有较大的差别,某些区域因电位较低而成为腐蚀微电池的阳极,而另外一些区域则作为阴极,从而形成数目繁多的微电池系统,造成锌在电池中的自腐蚀。自腐蚀不仅消耗了活性物质锌,减少了负极容量,而且气体的产生增加了电池内压,有可能引起蓄电池的电解液泄露,电池膨胀及使用寿命降低等问题。
为了提高锌电极析氢过电位,往往在电极中添加氢过电位较高的金属,最常用也是最有效的高氢过电位金属是汞或氧化汞。充电过程中,由于Hg/HgO电极电位较Zn/ZnO电极电位正,HgO先还原成Hg,还原的Hg与Zn形成合金(汞齐化),从而提高氢气在锌电极上的析出过电位,同时汞还可以使电极表面更加均匀。
根据以上机理分析,代汞添加剂应选择氢超电势较高的金属。研究较多的添加剂如金属Pb、In、Bi等,金属氧化物添加剂为PbO、Bi2O3、In2O3、Ti2O3与CdO,还有一些碱土金属的氢氧化物,其缓蚀机理同样是提高了氢的析出过电势,从而降低锌电极的腐蚀。
3国内外研究现状
3.1电极添加剂
锌电极添加剂不仅能降低锌电极的形变,也能有效的抑制枝晶生长,消除电流密度分布和锌酸盐浓度变化的不利影响。此类方法是在锌电极中加入氢过电势高的物质,锌电极在碱性溶液中的自放电就会明显降低,从而提高电池的性能。改善锌电极性能的电极添加剂分为金属单质添加剂、金属氧化物添加剂和氢氧化物添加剂。金属单质添加剂在碱性溶液中的平衡电位一般较锌正,在电极充电过程中优先沉积,在电极放电时这些添加剂一般不会溶解,主要是锌发生阳极溶解反应。由于外加金属具有较高的析氢过电位,抑制了阴极析氢反应的进行,因而有效的减缓了锌在碱性溶液中的腐蚀[9]。研究较多的金属添加剂为Bi、In、Cd、Pb、Mg、Tl等。金属氧化物添加剂及氢氧化物添加剂的作用是作为基底使锌在集流体上均匀沉积,同时改善锌电极的导电率。锌电极常用的金属氧化物添加剂包括HgO、Bi2O3、CdO、Tl2O3、PbO、SnO2、Ce2O3、La2O3、In2O3等。其中,铅、镉、铊和铟的氧化物能使电极上电流密度分布均匀,有效减小锌电极的形变;Bi2O3能较好地防止电解液的局部稠化使电极表面活性物质沉积更均匀,抑制枝晶生长。Ca(OH)2是锌电极中最常用的金属氢氧化物添加剂,Ca(OH)2可以减小锌电极在充放电过程中的形变,且氧化锌可与Ca(OH)2生成难溶于碱的锌酸钙,以此提高电极的电化学性能。Mg(OH)2、Al(OH)3和稀土氢氧化物近年来研究较多[10]。
石建珍[11]等认为单质In、Cd、Pb提高了锌电极的析氢过电位,具有很好的缓蚀作用,抑制了锌电极在碱性溶液中的自放电;但是这些金属对阳极极化有较大的影响,不能过多引入,以免在放电时造成锌电极钝化。毛瑞[12]认为镁能减缓或抑制电池在长期贮存过程中阳极的自溶。
Brookhaven国家实验室的许多科学家已经报道了Bi2O3作为锌负极作为添加剂的文章[13]。他们研究了Bi2O3作为负极唯一金属添加剂的小型镍/锌电池的循环性能。Bi2O3能够降低锌电极的形变,从而延长电池的循环寿命,主要是由于以下现象引起:
①Bi能够在较低的电位下沉积于集流体上;
②在锌沉积之前,有一定量的Bi2O3先还原;
③在ZnO上形成针状的网。
添加剂作为美国海军(NSWC,Carderock分部)资助的SBIR阶段Ⅰ项目和阶段Ⅱ项目[14-15]中的一部分,对其作了进一步研究工作。添加剂应用于小电池中,取得了令人兴奋的结果;但是大电池中,结果只比没有铋添加剂的对比电池好一点。试验表明,锌膏中加入大量的铋会带来不易混合的问题,尤其是在大批量制备的时候。为了解决这些问题,Yardney公司启动了升级设备及优化工艺过程的项目。通过该项目的实施,目前能够将不同铋含量的大批量锌膏混合均匀。与此同时,Yardney公司申请且被授予将添加剂应用于锌银电池中的专利[16]。
虽然许多金属氧化物都能明显改善锌电极的性能,但有些金属氧化物却会毒化锌电极。张海等[17]发现锌电极中添加HgO、Tl2O3、PbO、Bi2O3、CdO、In2O3、SnO2等金属氧化物时,显著地提高了Zn-Ni电池的循环寿命;而当添加Fe2O3、CuO、V2O5、Ga2O3、TiO2、WO2、MoO3等金属氧化物时,则明显地降低了Zn-Ni电池的循环寿命。
谭志勇[18]等研究了两种钙质添加剂Ca(OH)2与木质素磺酸钙对密封可充锌镍电池性能的影响。该研究认为,钙质添加剂可固定锌电极的放电产物,与锌酸根形成难溶的Ca[Zn(OH)3]2,可延长锌负极的寿命,改善锌镍电池的高温存放性能,提高荷电保持能力。徐松[19]等通过化学沉淀法在ZnO表面修饰了In(OH)3层,系统的研究了In(OH)3的负载量与循环寿命之间的关系,当负载量达到12.5%时,改善了ZnO的电化学性能。另外,孟宪玲[20]等人也曾研究在锌电极上覆盖一层稀土氢氧化物La(OH)3或Ce(OH)3膜,能有效抑制锌枝晶的生长和腐蚀等问题。
3.2电解液添加剂
电解液添加剂的使用十分广泛,电解液添加剂通常是一些平整剂、络合剂和表面活性剂,可以分为无机物、有机物及无机-有机联合使用的添加剂。作为电解液中无机物添加剂一般要求金属的沉积电位比锌正,从而在锌沉积前先还原成金属作为基底,利用金属材料的高导电性改善锌电极的导电率,这种基底效应使锌在集流体上形成均匀沉积,从而改善电流分布达到抑制枝晶生长的作用[9]。关于有机物添加剂的作用目前常用吸附理论[21]和电化学理论[21]来解释。吸附理论认为:有机分子在电极表面通过物理吸附和化学吸附生成连续的吸附层(分子膜),阻止了溶剂分子在电极表面的聚集,从而降低腐蚀和沉积反应速度。电化学理论认为;有机分子占据了腐蚀反应进行的活性位点,增大了反应的活化能;有机分子在电极/溶液界面上做定向排列,屏蔽了碱液与阳极的直接接触,从而达到抑制腐蚀的作用。电解液添加剂具有用量少、成本低、选择多、易于操作等优点。
Thornton和Carlson[22]认为,最为有效的电解液是具有最高电导率、同时OH-浓度最低的电解液。通常可以通过添加溶解度高的盐如硅酸盐、氰亚铁酸盐、氟化物等来达到。在这种情况下存在电池电阻增加、电池利用率降低的问题。循环寿命与能量密度之间的协调在选择添加剂时必须充分考虑。
曾冬青[23]等研究了有机添加剂六次甲基四胺(HT)、十二烷基苯磺酸钠(SDBS)、十六烷基三甲基溴化铵(CTAB)、亚硫酸钠(Na2SO3)以及他们的组合作为负极添加剂对密封AA型锌镍电池充放电、循环和自放电性能的影响,第50次循环(1C恒流充放电)的放电容量为设计容量(400mAh)的87.8%,常温存放28d后和50℃下存放7d后的放电容量是设计容量的82.8%和77.3%。
高鹏[24]等研究认为,当添加0.3%wt二乙醇胺+0.1%wt三乙醇胺时,锌电极综合性能优良,有望投入实际应用。
刘丽英[25]研究了锌电极在含有不同缓蚀剂的碱液中的电化学行为,发现一种阴离子表面活性剂N和一种非离子表面活性剂Y对锌负极具有明显的协同作用,复配缓蚀剂NY大大降低了锌电极的腐蚀,减少了析氢量,通过在锌电极表面发挥作用,抑制了枝晶的生长,且对锌电极放电性能影响不大。
3.3复合添加剂
因无机、有机添加剂具有各自的优点,研究者常致力于无机和有机添加剂的复合使用。Pb(NO3)2和有机缓蚀剂(十二烷基苯磺酸钠、十二烷基硫酸钠、六次甲基四胺)有很好的协同作用。周和兵[26]等采用量氢法研究了Pb(NO3)2与十
二烷基苯磺酸钠、十二烷基硫酸钠、六次甲基四胺三种有机缓蚀剂的组合使用对锌电极腐蚀的缓蚀效果。结果表明Pb(NO3)2和有机缓蚀剂单独使用时缓蚀效果比Hg差得多,但当Pb(NO3)2和单个有机缓蚀剂协调使用时,缓蚀效果比Hg好。
林海斌[27]等通过电化学方法、扫描电镜、放电测试等研究了Bi(NO3)2和有机缓蚀剂十二烷基苯磺酸钠(SDBS)的协同作用,当两者联合使用时,收到较好的抑制锌电极腐蚀的作用。单质金属Pb、Zn、Bi及含氟表面活性剂联合使用,具有良好的叠加效应,可以明显减小锌上的析氢电流密度,增大析氢超电势,减缓锌的腐蚀。胡经纬[28]等研究了铋与FC-170C、FSN、含氟阳离子型以及含氟两性表面活性剂组合对锌电极的缓释作用。发现其对锌电极的阳极过程产生明显的活化作用,提高阳极电流且能大幅增大大电流放电容量而不对阴极过程产生明显的影响。沈美芳[28]等采用循环伏安法和交流阻抗法实验发现表面活性剂四丁基溴化胺(C4H9)4NBr(TBAB)在锌电极的阴极还原过程中吸附在电极表面,能有效抑制锌电极在充电时产生枝晶,且Bi3+和TBAB对锌枝晶的抑制具有明显的协同作用。
4结论
综上所述,使用合适的锌电极及电解液添加剂可以有效地抑制锌的阳极析氢反应,减缓锌电极的腐蚀,抑制枝晶生长。但是,一些无机添加剂依然存在环境不友好、缓蚀作用差和钝化锌电极等缺点。而有机添加剂在碱性溶液中的稳定性不好,同时过多添加会降低电池性能。复合添加剂则是充分发挥无机和有机添加剂在锌电极和碱性电解液中的协同作用,因此,无机-有机复配添加剂将是锌电极缓蚀剂的研究重点。
目前,尽管科学工作者在锌电极及电解液添加剂方面已经取得一定的成效,但是对代汞缓蚀的机理研究具有较少的报道。在以后的工作中,应该在机理研究上多做工作,以便找到更好的代汞添加剂,早日在电池行业实现工业化。
参考文献
[1] Wagner O C, Himy A. Proc 28th Power Sources Symp. At-lantic City, NJ, 1978: 167.
[2] Choi K W; Bennion D N, Newman J.J Electrochem Soc, 1976, 123(11): 1616.
[3] McBreen J. J Electrochem Soc, 1972, 119(12): 1620.
[4] Einerhand R E F, Visscher W, Goeij J J M, etal. J Electrochem Soc, 1991, 138(1): 7.
[5] Despic A R, Diggle J, Bockris J O M. J Electrochem Soc, 1968, 115: 507~508.
[6] 吕鸣祥, 黄长保, 宋玉瑾编.化学电源. 天津: 天津大学出版社, 1992: 266~274.
[7] Diggle J W, Despic A R, Bockris J O M. J Appl Electrochem Soc, 1969, 116(11): 1503.
[8] 陈军, 陶占良, 苟兴龙. 化学电源. 北京: 化学工业出版社, 2006: 109.
[9] 王建明, 钱亚东, 张莉等.可充锌电极存在的问题及解决途径 J.电池, 1999, 29(2): 76~79.
[10] Sharma R.A. Kinetics of calcium zincate formation. J. Electrochem. Soc, 1988, 135(8): 1875~1882.
[11] 石建珍, 高翠琴, 朱纪凌等.电源技术, 1997, 21(2):3.
[12] 毛瑞.电池, 2001, 31(5): 236.
[13] J. McBreen, E. Gannon, Bismuth oxide as an additive in pasted zinc electrodes, J. Power Sources, 1985(15): 169~177.
[14] SBIR Phase I: Development of silver–zinc cells of improved cycle life and energy density, Contract N60921-91-C-0205, Aug. ’91, Report NSWCDD-TR-92/296.
[15] SBIR Phase II: Development of silver–zinc cells of improved cycle life and energy density, Contract N60921-93-C-0062, Jul. ’91, Report NSWCCD-TR-97/012.
[16] R. Serenyi, Yardney Technical Products, U.S. Patent No. 5,773,176, June 30, 1998.
[17] 张海, 王素卿.电池, 1992, 22(6): 24.
[18]谭志勇, 杨占红, 倪霞等. 钙质添加剂对密封可充锌镍电池性能的影响 J. 电池, 2012, 42(3): 153~155.
[19]徐松, 杨长春, 贺素娇等. 表面修饰In(OH)3后ZnO的电化学性能 J. 电池, 2009, 39(4): 195~197.
[20]孟宪玲, 杨化滨, 王军红等. 稀土氧化物对二次锌电极性能的影响 J. 电化学, 2005, 11(1): 58~61.
[21]朱厚军, 张伟东.碱性电池中锌阳极缓蚀剂应用研究 J. 船电技术, 2013, 33(5): 18~19.
[22] R.F.Thomton, E.J.Carlson. Properties of alternate electrolytes for secondary zinc batteries, J. Electrochem. Soc. 127(7)(1980): 1448~1452.
[23]曾东青, 杨占红, 王升威等. 电解液用量及负极添加剂对锌镍电池的影响 J.电池, 2010, 40(6): 306~309.
[24]高鹏, 董媛媛, 张哲等.二乙醇胺、三乙醇胺对锌电极性能的影响 J. 电池工业, 2011, 16(1):13~17.
[25]刘丽英, 郭炳焜, 徐徽等. 高效复配有机代汞缓蚀剂的研究 J. 电源技术, 2000, 25(4): 257~259.
[26]周合兵, 杨美珠, 吕东生等. KOH中几种缓蚀剂抑制锌腐蚀的协同作用 J. 电源技术, 2002, 26(149): 195~197.
[27]林海斌, 洪淑娜, 梁曼等. KOH溶液中添加剂影响锌电化学性能的研究 J. 电源技术, 2011, 35(10): 1227~1230.
[28]朱厚军, 张伟东. 碱性电池中锌阳极缓蚀剂应用研究 J. 船电技术, 2013, 33(5): 17~19.
编辑:《电源工业》杂志
来源:樊兆宝、刘丽娟、何玉彬/贵州梅岭电源
标签:
下一篇:真空和膏工艺对电池性能的影响
相关信息
MORE >>-
伊顿 SwitchGard 局放监测成功预警,护航海上电力动力平台稳健运行
近期,安装于某海上平台分段隔离柜的伊顿 SwitchGard 局放监测装置,成功捕捉到柜内异常放电信号,并提供了准确的 PRPD 局放检测图谱分析结果,为故障定位和后续检修赢得了宝贵的时间窗口,避免了非计划停机可能带来的经济损失与安全风险。
-
迈向长距离运输脱碳之路
LEM作为电量测量领域的专注者,其直流计费表DCBM系列产品旨在简化电表集成到充电桩的过程,为直流快速充电和直流目标充电系统提供解决方案。LEM电动汽车充电和计量全球产品经理Florent Balboni详细介绍了电动卡车充电的挑战以及对准确电量计量的需求。
-
达人观点 | 分布式-集中式控制引领运动控制技术的未来
image.png
作为台达工业自动化技术体系的重要开拓者之一,蔡清雄博士以三十年深耕铸就了台达在运动控制领域的领先地位。凭借对未来工业发展的深刻洞察,蔡清雄博士提出了“分布式-集中式控制将是运动控制技术未来革新的方向”。 -
IO-Link如何将“智能”融入智能工厂
Analog Devices, Inc. (NASDAQ: ADI)是全球领先的半导体公司,致力于在现实世界与数字世界之间架起桥梁,以实现智能边缘领域的突破性创新。
-
巨磁阻多圈位置传感器的磁体设计
Analog Devices, Inc. (NASDAQ: ADI)是全球领先的半导体公司,致力于在现实世界与数字世界之间架起桥梁,以实现智能边缘领域的突破性创新。
-
提升视觉体验:MIPI DSI-2赋能新一代AR/VR
通过MIPI技术和Rambus经过优化的MIPI DSI-2控制器内核的功能,产品设计人员可以更加从容地应对AR/VR设备在高性能数据传输、低延迟和高能效方面的挑战,最终提供更好的用户体验。









 中国电源产业网网友交流群:2223934、7921477、9640496、11647415
中国电源产业网网友交流群:2223934、7921477、9640496、11647415